2025年05月28日成考高起点每日一练《理化综合》
成考高起点 2025-05-28作者:匿名 来源:本站整理
2025年成考高起点每日一练《理化综合》5月28日专为备考2025年理化综合考生准备,帮助考生通过每日坚持练习,逐步提升考试成绩。
单选题
1、实验室里分别制取下列各组中的气体,可采用同一种气体发生装置制取的气体是()。
- A:O2、CO2、H2
- B:H2、Cl2、C2H4
- C:NH3、CO2、Cl2
- D:NH3、CH4、O2
答 案:D
解 析:解答此题主要考虑两个条件:①制取气体的反应类型要相同。如“固+固→气”与“固+液→气”,其反应类型不同,采用的制取装置也不可能相同。②反应条件要相同。如“固+液→气”这一类型中,有加热和不加热之分。反应条件不同,采用的制取装置也不可能相同,在D选项中,制取NH3、CH4、O2都属于“固十固→气”一类,且均需加热。所以D选项正确。
2、人在岸上看到河中的鱼,其实看到的是()
- A:鱼的实像,其位置比鱼的实际位置浅
- B:鱼的实像,其位置比鱼的实际位置深
- C:鱼的虚像,其位置比鱼的实际位置浅
- D:鱼的虚像,其位置比鱼的实际位置深
答 案:C
解 析:水对光有折射作用,如右图所示,人眼看到的是鱼的虚像,虚像比实际位置浅。 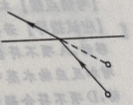
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、工业上用焙烧NaHCO3的方法生产纯碱(Na2CO3)。现有17.5g的NaHCO3样品,加热分解完全后,生成标准状况下的CO2气体2.24L。写出NaHCO3分解反应的化学方程式,计算此NaHCO3样品的纯度。
答 案:NaHCO3分解反应的化学方程式如下: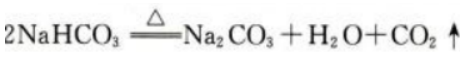 反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
2、实验室选用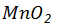 与10mol/L浓盐酸反应制备氯气,其化学反应方程式是 ,
与10mol/L浓盐酸反应制备氯气,其化学反应方程式是 ,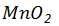 在反应中作 (填“氧化剂”或“还原剂”);若生成标准状况下氯气2.8L,反应中转移电子多少摩尔?消耗该盐酸溶液多少毫升?
在反应中作 (填“氧化剂”或“还原剂”);若生成标准状况下氯气2.8L,反应中转移电子多少摩尔?消耗该盐酸溶液多少毫升?
答 案:
解 析:
填空题
1、物体在力F作用下做加速运动,当力F逐渐减小时,物体的加速度______,速度______。当F减小到零时,物体的加速度将______,速度将______(填“变大”“变小”“不变”“最大”“最小”或“等于零”)。
答 案:变小;变大;等于零;不变
2、同温同压下与4gH2气体体积相同的O2气体为()g。
答 案:64
简答题
1、某气态烃与过量的O2混合物共10L,点燃反应后,气体混合物仍为10L,通过浓H2SO4后体积变6L,再通过NaOH,体积变成2L(气体体积均在同一状况下测定,且此条件下水为气态).求该烃的分子式,并写出结构简式,指出所属有机物类别
答 案:反应后产生的水蒸气其体积为10L-6L=4L, CO2的体积为10L-4L-2L=4L,剩余的2L气体为未反应的O2体积,
因为每生成1体积CO2消耗1体积O2,每生成1体积水蒸气消耗0.5体积O2,故反应掉的O2体积是4L+2L=6L.
则反应前混合气体中O2的体积为6L+2L=81,烃的体积为10L-8L=2L设气态烃的分子式为CXHY,则
2、在相同条件下,0.1molZn和0.1molAl分别跟足量的稀盐酸反应,哪个反应放出的氢气多?
答 案:锌和铝分别跟稀盐酸反应的化学方程式是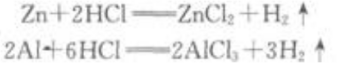 从方程式可知1molZn跟足量的稀盐酸反应,可以放出1molH2;1mol Al跟足量的稀盐酸反应,可以放出1.5 mol H2.由此可知,0.1mol AI跟足量的稀盐酸反应放出的氢气比0.1molZn放出的多.
答:0.1mol AI与足量的稀盐酸反应放出的氢气多
从方程式可知1molZn跟足量的稀盐酸反应,可以放出1molH2;1mol Al跟足量的稀盐酸反应,可以放出1.5 mol H2.由此可知,0.1mol AI跟足量的稀盐酸反应放出的氢气比0.1molZn放出的多.
答:0.1mol AI与足量的稀盐酸反应放出的氢气多